癌细胞如何修复下一代放疗引起的DNA损伤
由基础科学研究所(IBS) 基因组完整性中心 (CGI) 的 Kei-ichi TAKATA 博士领导的科学家团队发现了一种新型 DNA 修复机制,癌细胞可利用该机制从下一代恢复癌症放射治疗。
电离辐射 (IR) 疗法经常用于治疗癌症,并被认为可以通过诱导 DNA 断裂来破坏癌细胞。最新类型的放射治疗利用粒子加速器产生的辐射,粒子加速器由带电重粒子(例如碳离子)组成。粒子加速器将碳离子加速到光速的 70% 左右,与癌细胞的 DNA 碰撞并破坏。
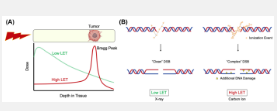
这些离子具有高线性能量转移 (LET),并在称为布拉格峰的短距离内释放大部分能量。下一代癌症放疗的工作原理是将布拉格峰聚焦在肿瘤上,与常用的低 LET 辐射(例如伽马射线或 X 射线)相比,它的额外好处是可以最大程度地减少对周围正常组织的损害(图 1A )。
目前世界上只有少数医疗机构具备提供这种下一代放射治疗的能力,尽管未来有望部署更多医疗机构。
重离子轰击(高 LET 辐射)产生的 DNA 损伤比传统放射治疗(低 LET 辐射)引起的损伤更“复杂”。前者携带额外的 DNA 损伤,例如靠近双链断裂 (DSB) 位点的脱嘌呤/脱嘧啶 (AP) 位点和胸腺嘧啶乙二醇 (Tg),这比普通 DNA 损伤更难修复。因此,与低 LET 辐射相比,先进疗法每单位剂量的细胞毒性更大(图 1B)。
这使得下一代放射疗法成为对抗癌细胞的有力武器。然而,尚未完全研究这些高 LET 诱导的损伤是如何在哺乳动物细胞中处理的,因为重离子轰击造成的 DNA 损伤是自然界中很少发生的过程(例如,在外太空发生的几率更高)。弄清楚复杂的 DSB 修复机制是一个有吸引力的研究兴趣,因为阻断癌细胞的修复机制可以使新的放射疗法变得更加有效。
为了进行研究,IBS团队访问了日本QST医院,使用了名为HIMAC(千叶重离子医学加速器)的同步加速器,该加速器具有产生高LET辐射的能力。延世大学已经安装了一个类似的同步加速器,另一个计划于 2027 年在 Kijang 的首尔国立大学医院安装。高田博士的研究团队打算帮助在韩国建立一个使用这些同步加速器的基础研究计划,以改善重离子癌症患者的治疗。
高田博士的研究小组发现,DNA 聚合酶 θ (POLQ) 是修复复杂 DSB 的重要因素,例如由重离子轰击引起的 DSB。POLQ 是一种独特的 DNA 聚合酶,能够跨脱碱基 (AP) 位点和胸腺嘧啶乙二醇 (Tg) 执行微同源介导的末端连接以及转位合成 (TLS)。发现此 TLS 活动是允许复杂 DSB 修复的生物学重要因素。
共同第一作者之一的 SUNG Yubin 女士解释说:“我们提供的证据表明,POLQ 的 TLS 活性在修复 hiLET-DSB 中起着关键作用。我们发现 POLQ 可以有效地退火和延伸模仿复杂 DSB 的底物”(图 2)。
研究人员还发现,阻止癌细胞中 POLQ 的表达大大增加了它们对新放射治疗的脆弱性。
“我们证明了POLQ的遗传破坏导致染色单体断裂增加,并在高 LET 辐射处理后增强了细胞敏感性,”另一位联合第一作者 YI Geunil 先生解释道(图3)。
研究团队利用生化技术和荧光共振能量转移 (FRET) 发现 POLQ 蛋白可以有效修复模拟复杂 DSB 的合成 DNA 分子。这意味着 POLQ 可能成为增加癌细胞抵抗复杂辐射损伤的脆弱性的新药物靶点。
用于监测 POLQ 介导的退火和 DNA 延伸的单分子 FRET 分析系统是与 UNIST 的 KIM Hajin 教授和 KIM Chanwoo 先生合作开发的。IBS-CGI 的 RA Jae Sun 女士分析了高 LET 辐射引起的染色单体断裂。QST 的 FUJIMORI Akira 教授和 HIRAKAWA Hirokazu 先生以及科罗拉多州立大学的 KATO Takamitsu 教授帮助使用 HIMAC 进行了实验。
Takata 教授指出:“我们很自豪地宣布我们的论文发表,这只有通过所有相关人员的出色团队合作才能实现。我们的发现为 hiLET-DSB 在哺乳动物细胞中的修复机制提供了新的见解,并进一步表明抑制 POLQ 可能会增强重离子放射治疗的疗效。”
这项工作于 2023 年 2 月 20 日发表在Nucleic Acids Research上。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
2025年6月20日,——在世界文化遗产地河南洛阳的光影流转之间,2025年新浪微博旅游之夜盛大举行。作为国内首个...浏览全文>>
-
2025年6月20日,——在世界文化遗产地河南洛阳的光影流转之间,2025年新浪微博旅游之夜盛大举行。作为国内首个...浏览全文>>
-
QQ多米试驾线下预约活动为了让更多用户感受QQ多米的独特魅力,我们特别推出了线下试驾预约活动。这不仅是一次...浏览全文>>
-
阜阳长安启源A07以其卓越的性能和豪华配置吸引了众多消费者的目光。作为一款定位高端市场的新能源车型,长安启...浏览全文>>
-
【安徽淮南大众CC新车报价2025款大公开】大众CC作为一款兼具运动感与豪华质感的轿跑车型,一直深受消费者喜爱...浏览全文>>
-
2025款长安猎手K50在安徽淮南地区的最新价格已新鲜出炉,为准备购车的朋友带来全面解析。这款车型以其高性价比...浏览全文>>
-
在安徽滁州购买长安猎手K50时,了解其落地价和省钱技巧至关重要。长安猎手K50是一款实用性强的皮卡车型,适合...浏览全文>>
-
途锐新能源是大众旗下的一款高端插电混动SUV,目前在安徽阜阳地区有售。其官方指导价约为58万元起,但实际成交...浏览全文>>
-
2025款大众CC作为一款兼具运动与豪华的中型轿车,备受关注。目前市场指导价大约在25万至35万元之间,具体价格...浏览全文>>
-
2024款探岳X作为一款备受关注的中型SUV,在市场上以其时尚的设计和出色的性能吸引了众多消费者。根据最新市场...浏览全文>>
- QQ多米试驾线下预约
- 安徽滁州长安猎手K50落地价,买车省钱秘籍
- 淮南大众CC新款价格2025款多少钱?买车攻略一网打尽
- 瑞虎8 PRO试驾,畅享豪华驾乘,体验卓越性能
- 安徽阜阳长安启源A05多少钱 2025款落地价,换代前的购车良机,不容错过
- 保时捷Macan试驾的流程是什么
- 安徽淮南大众ID.3多少钱?购车攻略在此
- 阜阳揽巡落地价,豪华配置超值价来袭
- 安徽池州威然 2024新款价格与配置的完美平衡
- 奇瑞瑞虎9试驾,新手必知的详细步骤
- QQ多米价格,换代前的购车良机,不容错过
- 池州迈腾GTE新款价格2022款多少钱?选车秘籍与优惠全公开
- 岚图追光多少钱 2024款落地价走势,近一个月最低售价25.28万起,性价比凸显
- 天津滨海威然 2024新款价格,最低售价28.98万起,入手正当时
- 蚌埠途昂新款价格2025款多少钱?购车必看
- 坦克400预约试驾全攻略
- 天津滨海ID.7 VIZZION价格,各配置车型售价全揭晓,性价比之王
- 安庆帕萨特最新价格2025款,最低售价12.35万起,入手正当时
- 亳州宝来新款价格2025款多少钱?选车指南与落地价全解析
- 生活家PHEV 2025新款价格,最低售价63.98万起现在该入手吗?
