首页 >> 综合 > 精选知识 >
细胞源性纳米载体可实现更有效更直接的细胞内药物释放
在药物递送中,纳米载体的治疗行为受到其表面的“外来”特征的限制。尽管有多种复杂的涂层可供选择,但免疫细胞通常会识别这些合成纳米颗粒,从而产生不良反应或表现出强烈的脱靶积累。从这个意义上说,仿生材料的使用成为规避这种认识并提高输送系统有效性的替代方案。利用同型特性,仿生载体对细胞微环境表现出更高的亲和力和有价值的免疫逃逸能力。
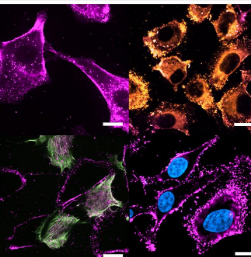
这种方法促使生物化学和分子材料研究中心 (CiQUS) 的研究人员模仿肿瘤细胞的膜组成,并开发出新的脂质纳米载体,该载体与宿主细胞膜融合以释放生物活性分子。嵌入仿生壳中的阳离子(带正电)和中性脂质的非常精确的组合为纳米载体提供了这种融合特性,并促进其与质膜的结合:“通过结合融合特性和仿生特征,我们实现了几种类型有效负载的细胞内定位,从小分子到大分子和固体纳米粒子” ,CiQUS研究员、生物纳米工具组。这种融合允许药物和其他感兴趣的分子直接释放到胞质溶胶中,从而增强递送系统的治疗功效和所运输的化合物的生物利用度。
BioNanoTools专注于开发用于生物学和医学应用的多功能复合材料。现在,CiQUS 研究人员为新系统提供了双重功能,旨在比更传统的方法提高药物输送的选择性和安全性:“由于其同型特性,这些细胞衍生的纳米载体具有很高的选择性。另一方面,由脂质的特定组合提供的融合能力使得货物的释放更加有效”。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
分享:
最新文章
-
2025年6月20日,——在世界文化遗产地河南洛阳的光影流转之间,2025年新浪微博旅游之夜盛大举行。作为国内首个...浏览全文>>
-
2025年6月20日,——在世界文化遗产地河南洛阳的光影流转之间,2025年新浪微博旅游之夜盛大举行。作为国内首个...浏览全文>>
-
QQ多米试驾线下预约活动为了让更多用户感受QQ多米的独特魅力,我们特别推出了线下试驾预约活动。这不仅是一次...浏览全文>>
-
阜阳长安启源A07以其卓越的性能和豪华配置吸引了众多消费者的目光。作为一款定位高端市场的新能源车型,长安启...浏览全文>>
-
【安徽淮南大众CC新车报价2025款大公开】大众CC作为一款兼具运动感与豪华质感的轿跑车型,一直深受消费者喜爱...浏览全文>>
-
2025款长安猎手K50在安徽淮南地区的最新价格已新鲜出炉,为准备购车的朋友带来全面解析。这款车型以其高性价比...浏览全文>>
-
在安徽滁州购买长安猎手K50时,了解其落地价和省钱技巧至关重要。长安猎手K50是一款实用性强的皮卡车型,适合...浏览全文>>
-
途锐新能源是大众旗下的一款高端插电混动SUV,目前在安徽阜阳地区有售。其官方指导价约为58万元起,但实际成交...浏览全文>>
-
2025款大众CC作为一款兼具运动与豪华的中型轿车,备受关注。目前市场指导价大约在25万至35万元之间,具体价格...浏览全文>>
-
2024款探岳X作为一款备受关注的中型SUV,在市场上以其时尚的设计和出色的性能吸引了众多消费者。根据最新市场...浏览全文>>
大家爱看
频道推荐
站长推荐
- QQ多米试驾线下预约
- 安徽滁州长安猎手K50落地价,买车省钱秘籍
- 淮南大众CC新款价格2025款多少钱?买车攻略一网打尽
- 瑞虎8 PRO试驾,畅享豪华驾乘,体验卓越性能
- 安徽阜阳长安启源A05多少钱 2025款落地价,换代前的购车良机,不容错过
- 保时捷Macan试驾的流程是什么
- 安徽淮南大众ID.3多少钱?购车攻略在此
- 阜阳揽巡落地价,豪华配置超值价来袭
- 安徽池州威然 2024新款价格与配置的完美平衡
- 奇瑞瑞虎9试驾,新手必知的详细步骤
- QQ多米价格,换代前的购车良机,不容错过
- 池州迈腾GTE新款价格2022款多少钱?选车秘籍与优惠全公开
- 岚图追光多少钱 2024款落地价走势,近一个月最低售价25.28万起,性价比凸显
- 天津滨海威然 2024新款价格,最低售价28.98万起,入手正当时
- 蚌埠途昂新款价格2025款多少钱?购车必看
- 坦克400预约试驾全攻略
- 天津滨海ID.7 VIZZION价格,各配置车型售价全揭晓,性价比之王
- 安庆帕萨特最新价格2025款,最低售价12.35万起,入手正当时
- 亳州宝来新款价格2025款多少钱?选车指南与落地价全解析
- 生活家PHEV 2025新款价格,最低售价63.98万起现在该入手吗?
