破译我们细胞的高速公路密码
癌症、退行性疾病:细胞内部通讯途径的失调是许多疾病的根源。微管——微观蛋白质丝——在控制这些交换中发挥着至关重要的作用。然而,它们的机制仍然知之甚少。日内瓦大学 (UNIGE) 的一个团队发现了一种新机制,涉及两种蛋白质,可以控制它们的生长。这一发现为开发可作用于细胞核心的新疗法开辟了前所未有的前景。这些结果发表在《 美国国家科学院院刊》(PNAS)上。
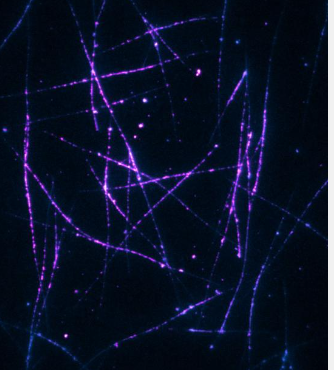
正如城市需要流动的交通网络来进行交流和发展一样,细胞也需要内部微观的“道路”来供给自身、生长和分裂。这些“道路”被称为“微管”。它们是形成细胞主干的长蛋白质丝。它们的调节问题可能会导致癌症和神经退行性疾病等疾病。
因此,了解它们的工作原理,特别是控制和调节它们生长的机制,至关重要。尽管过去四十年来该领域取得了重大进展,但该系统的复杂性仍然需要深入研究。
两个关键蛋白质
UNIGE 理学院生物化学系助理教授 Charlotte Aumeier 最近的工作为微管的功能提供了新的见解。它显示了两种特定蛋白质 CLIP-170 和 EB3 在生长过程中如何在微管尖端进行液-液相分离。换句话说,这两种蛋白质与细胞液体介质分离,在微管尖端形成第二液相,就像水中的一滴油。
微管是不断构建和解构自身的动态结构。“微管水平上的这种相分离现象增加了蛋白质(包括微管蛋白)的浓度,并显着刺激微管的生长速度,同时减少解聚事件,即微管衰变事件,”最后一位研究人员夏洛特·奥梅尔(Charlotte Aumeier)解释道。该研究的作者。因此,这种机制似乎以非常具体的方式控制细胞微管的动力学。
联合行动
Charlotte Aumeier 实验室的博士生、该研究的第一作者 Julie Miesch 解释说,“正是 CLIP-170 和 EB3 之间的协同作用确保了微管生长的调节,这要归功于液-液相分离机制” 。单独来看,CLIP-170 与微管蛋白没有相互作用。至于EB3,虽然它能够与微管蛋白相互作用,但它仅在表面形成微小的聚集体。这两种蛋白质的结合使得局部调节微管生长的速度成为可能。
通过体外观察这两种蛋白质的作用,然后使用全内反射荧光显微镜和高通量共聚焦显微镜这两种方法的组合进行纤维素测量,这两种方法可在 ACCESS GENEVA 平台的 UNIGE 上 获得 。
这些结果凸显了微管动力学控制的新水平。这为开发新的抗癌疗法开辟了新靶点的可能性。这一突破有望进一步拓宽我们对细胞过程核心的理解和行动能力。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
2025年6月20日,——在世界文化遗产地河南洛阳的光影流转之间,2025年新浪微博旅游之夜盛大举行。作为国内首个...浏览全文>>
-
2025年6月20日,——在世界文化遗产地河南洛阳的光影流转之间,2025年新浪微博旅游之夜盛大举行。作为国内首个...浏览全文>>
-
QQ多米试驾线下预约活动为了让更多用户感受QQ多米的独特魅力,我们特别推出了线下试驾预约活动。这不仅是一次...浏览全文>>
-
阜阳长安启源A07以其卓越的性能和豪华配置吸引了众多消费者的目光。作为一款定位高端市场的新能源车型,长安启...浏览全文>>
-
【安徽淮南大众CC新车报价2025款大公开】大众CC作为一款兼具运动感与豪华质感的轿跑车型,一直深受消费者喜爱...浏览全文>>
-
2025款长安猎手K50在安徽淮南地区的最新价格已新鲜出炉,为准备购车的朋友带来全面解析。这款车型以其高性价比...浏览全文>>
-
在安徽滁州购买长安猎手K50时,了解其落地价和省钱技巧至关重要。长安猎手K50是一款实用性强的皮卡车型,适合...浏览全文>>
-
途锐新能源是大众旗下的一款高端插电混动SUV,目前在安徽阜阳地区有售。其官方指导价约为58万元起,但实际成交...浏览全文>>
-
2025款大众CC作为一款兼具运动与豪华的中型轿车,备受关注。目前市场指导价大约在25万至35万元之间,具体价格...浏览全文>>
-
2024款探岳X作为一款备受关注的中型SUV,在市场上以其时尚的设计和出色的性能吸引了众多消费者。根据最新市场...浏览全文>>
- QQ多米试驾线下预约
- 安徽滁州长安猎手K50落地价,买车省钱秘籍
- 淮南大众CC新款价格2025款多少钱?买车攻略一网打尽
- 瑞虎8 PRO试驾,畅享豪华驾乘,体验卓越性能
- 安徽阜阳长安启源A05多少钱 2025款落地价,换代前的购车良机,不容错过
- 保时捷Macan试驾的流程是什么
- 安徽淮南大众ID.3多少钱?购车攻略在此
- 阜阳揽巡落地价,豪华配置超值价来袭
- 安徽池州威然 2024新款价格与配置的完美平衡
- 奇瑞瑞虎9试驾,新手必知的详细步骤
- QQ多米价格,换代前的购车良机,不容错过
- 池州迈腾GTE新款价格2022款多少钱?选车秘籍与优惠全公开
- 岚图追光多少钱 2024款落地价走势,近一个月最低售价25.28万起,性价比凸显
- 天津滨海威然 2024新款价格,最低售价28.98万起,入手正当时
- 蚌埠途昂新款价格2025款多少钱?购车必看
- 坦克400预约试驾全攻略
- 天津滨海ID.7 VIZZION价格,各配置车型售价全揭晓,性价比之王
- 安庆帕萨特最新价格2025款,最低售价12.35万起,入手正当时
- 亳州宝来新款价格2025款多少钱?选车指南与落地价全解析
- 生活家PHEV 2025新款价格,最低售价63.98万起现在该入手吗?
