齐心协力抗击癌症
神经内分泌肿瘤,包括小细胞肺癌和神经内分泌前列腺癌,具有极强的侵袭性,扩散的可能性很高。然而,许多患者对少数可用治疗方法产生了耐药性,导致患者预后不佳。因此,研究人员旨在开发新的治疗方法,重点关注这些肿瘤的疾病特异性分子机制。
大阪大学的一组研究人员在最近发表在《分子治疗:核酸》上的一篇文章中描述了一种针对这种机制(即 RNA 剪接)的策略。
RNA 剪接是细胞去除信使 RNA (mRNA) 分子某些部分的过程。这会产生成熟的 mRNA,其中包含制造特定基因蛋白质的指令。由于错误的 RNA 剪接会导致蛋白质功能失调或过度活跃,因此该过程可能极大地促进疾病的发展。
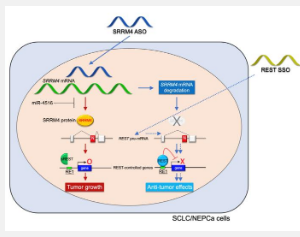
该团队重点研究了一种名为 RE1 沉默转录因子 (REST) 的蛋白质,该因子通常会抑制支持神经内分泌表型的某些基因。有趣的是,REST mRNA 的异常剪接形式在神经内分泌肿瘤中表达水平较高。
“REST mRNA 的错误剪接会导致产生的蛋白质失去功能,从而导致神经内分泌癌的发展,”该研究的主要作者 Keishiro Mishima 说道。“我们小组的目标是开发一种可用于纠正 REST 剪接模式的分子方法。”
研究团队使用了一种名为酰胺桥核酸剪接转换寡核苷酸 (SSO) 的分子。这些 SSO 旨在与 REST mRNA 分子的特定部分相互作用,使其剪接回正常形式。研究人员将神经内分泌癌细胞植入实验室小鼠的皮下以形成肿瘤。然后,他们将盐水或 SSO 注射到小鼠的腹部,监测肿瘤生长情况并收集血液样本。
“我们检查了小鼠血清样本中某些生化标志物的水平,以确保 SSO 治疗不会引起任何肝性,”资深作者 Masahito Shimojo 解释说,“同时,我们用 SSO 处理培养的神经内分泌癌细胞系,以获得体外数据来支持我们的体内发现。”
REST SSO 治疗导致存活癌细胞的数量比对照治疗少得多。此外,注射 REST SSO 的小鼠的肿瘤大小显著减小。研究小组随后进行了进一步的分子分析,以检查 REST 在正常条件下通常会抑制的基因的表达模式。
“治疗后,与对照组相比,SSO 治疗的肿瘤中 REST 控制的基因表达水平显著下降,”Shimojo 说。“这表明 SSO 促进了 REST 功能的恢复。”
总的来说,该研究表明这种独特、新颖的治疗方法对治疗难治性神经内分泌癌具有良好的前景。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
2025年6月20日,——在世界文化遗产地河南洛阳的光影流转之间,2025年新浪微博旅游之夜盛大举行。作为国内首个...浏览全文>>
-
2025年6月20日,——在世界文化遗产地河南洛阳的光影流转之间,2025年新浪微博旅游之夜盛大举行。作为国内首个...浏览全文>>
-
QQ多米试驾线下预约活动为了让更多用户感受QQ多米的独特魅力,我们特别推出了线下试驾预约活动。这不仅是一次...浏览全文>>
-
阜阳长安启源A07以其卓越的性能和豪华配置吸引了众多消费者的目光。作为一款定位高端市场的新能源车型,长安启...浏览全文>>
-
【安徽淮南大众CC新车报价2025款大公开】大众CC作为一款兼具运动感与豪华质感的轿跑车型,一直深受消费者喜爱...浏览全文>>
-
2025款长安猎手K50在安徽淮南地区的最新价格已新鲜出炉,为准备购车的朋友带来全面解析。这款车型以其高性价比...浏览全文>>
-
在安徽滁州购买长安猎手K50时,了解其落地价和省钱技巧至关重要。长安猎手K50是一款实用性强的皮卡车型,适合...浏览全文>>
-
途锐新能源是大众旗下的一款高端插电混动SUV,目前在安徽阜阳地区有售。其官方指导价约为58万元起,但实际成交...浏览全文>>
-
2025款大众CC作为一款兼具运动与豪华的中型轿车,备受关注。目前市场指导价大约在25万至35万元之间,具体价格...浏览全文>>
-
2024款探岳X作为一款备受关注的中型SUV,在市场上以其时尚的设计和出色的性能吸引了众多消费者。根据最新市场...浏览全文>>
- QQ多米试驾线下预约
- 安徽滁州长安猎手K50落地价,买车省钱秘籍
- 淮南大众CC新款价格2025款多少钱?买车攻略一网打尽
- 瑞虎8 PRO试驾,畅享豪华驾乘,体验卓越性能
- 安徽阜阳长安启源A05多少钱 2025款落地价,换代前的购车良机,不容错过
- 保时捷Macan试驾的流程是什么
- 安徽淮南大众ID.3多少钱?购车攻略在此
- 阜阳揽巡落地价,豪华配置超值价来袭
- 安徽池州威然 2024新款价格与配置的完美平衡
- 奇瑞瑞虎9试驾,新手必知的详细步骤
- QQ多米价格,换代前的购车良机,不容错过
- 池州迈腾GTE新款价格2022款多少钱?选车秘籍与优惠全公开
- 岚图追光多少钱 2024款落地价走势,近一个月最低售价25.28万起,性价比凸显
- 天津滨海威然 2024新款价格,最低售价28.98万起,入手正当时
- 蚌埠途昂新款价格2025款多少钱?购车必看
- 坦克400预约试驾全攻略
- 天津滨海ID.7 VIZZION价格,各配置车型售价全揭晓,性价比之王
- 安庆帕萨特最新价格2025款,最低售价12.35万起,入手正当时
- 亳州宝来新款价格2025款多少钱?选车指南与落地价全解析
- 生活家PHEV 2025新款价格,最低售价63.98万起现在该入手吗?
